2014年3月5日
骨粗しょう症メカニズム解明への一歩
私たちの体を支える骨格は、骨組織を壊し、血液中のカルシウム濃度を高める破骨細胞と、血液中のカルシウムを取り込み、骨に蓄える骨芽細胞の働きのバランスにより新陳代謝を行っています。この代謝は主にホルモンにより調節されているほか、近年CNOTという細胞内タンパク質の関与が明らかになってきました。CNOTは現在、CNOT1からCNOT11までの11種類が確認されており、細胞内で余分になったmRNA(メッセンジャーRNA)を処理し、機能タンパク質の過剰な産生を抑制する働きがあると分かっています。また、それぞれのCNOTの欠損が様々な疾患を引き起こすと考えられ、研究が進められています。
哺乳類CNOTの生体内での機能とそのメカニズムにいち早く着眼し、基礎研究を始めたのが、OIST細胞シグナルユニットの山本雅教授のグループです。山本教授は初め、外部環境を受容するタンパク質が、mRNAを分解する働きを持つCNOTに情報を伝え、遺伝子の発現の調節(転写後調節)にも関わると指摘しました。さらに各CNOTの働きを解明することで、生体の恒常性維持の仕組みの一端が分かるのではないかと考えて研究を進めています。具体的には、特定のCNOTの働きを遺伝子的に様々なレベルで抑制したマウスの特徴を仔細に調べてきました。
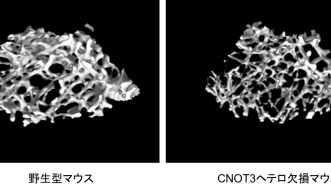
2月4日、東京医科歯科大学の野田政樹教授率いる研究チームは、加齢で骨粗しょう症が引き起こされる仕組みについて、CNOTの一つであるCNOT3が重要であるという研究成果を発表しました。骨研究の専門家である野田教授は、細胞シグナルユニットと協力してCNOT3と骨代謝の関係を追求し、CNOT3の発現が抑制されたマウスでは骨が脆弱であることを見いだしました。さらにCNOT3が、破骨細胞の表面に発現するRANKというレセプターを産出するmRNAを分解する働きがあることを明らかにしました。そのためCNOT3の欠乏は、RANKレセプターの産生と活性を高め、破骨細胞の働きも活性化します。この研究成果により、老齢者の骨組織でCNOT3の発現が減少すると骨密度の低下が引き起こされ、骨粗しょう症に至る一因となっていることが示唆されました。
OIST細胞シグナルユニットは、CNOTの働きの全体像を分子レベルで追及すると共に、これまでの研究成果の情報や遺伝子改変マウスの提供、CNOTの発現解析方法の提案を惜しまずに行っています。「それぞれの専門性を活かし、様々な生命現象の仕組みが解明されると良いと思います。そして様々な疾患のメカニズムがCNOTとの関連性を通じて解明されるものと期待しています」と山本教授は語っています。
西岡 真由美