2024年6月20日
アルツハイマー病によるシナプスへのダメージを回復
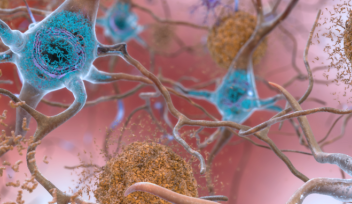
アルツハイマー病は、進行性の神経変性疾患であり、認知機能の低下、記憶力の低下、そして最終的には日常生活が送れなくなる認知症の主な原因となっています。全世界で推定5500万人、日本では推定440万人が認知症を患っているとされており、日本政府のデータによると、その数は2060年には650万人にまで増加すると予想されています。
アルツハイマーの症状を治したり、遅らせたりすることは、この病気のとらえどころのない性質のため非常に困難です。正確な原因は不明で、遺伝から生活習慣まで、複数の要因が関与している可能性が高いとされています。また、症状が進行性であるため、日常生活に影響が出始めてからでは手遅れになることが多いのです。
この度、高橋智幸名誉教授が率いる沖縄科学技術大学院大学(OIST)の細胞分子シナプス機能ユニット(2024年3月末まで)の研究チームは、このような症状に対する有効な治療法を発見し、アルツハイマー病によって脳の機能が非可逆的に損なわれる前に、脳の機能を回復させる道を切り開きました。この研究成果は、科学誌『Brain Research』に掲載されました。本研究の筆頭著者で、現在はOIST神経計算ユニット所属するチャジュン・チャン博士は、「本研究では、アルツハイマー病にかかったマウスの症状の進行を逆転させることに成功しました。これを達成するために、小分子である合成ペプチドPHDP5を用いました。合成ペプチドPHDP5は血液脳関門を容易に通過して脳に直接作用ます」と説明します。
ダイナミンを救う
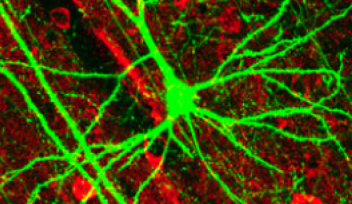
アルツハイマー病の中心的な要因は、脳のシナプスの健康状態です。シナプスとは、脳の神経細胞(ニューロン)間の接合部のことで、神経情報がシナプス小胞内の化学伝達物質を介し神経細胞から別の神経細胞へと伝達されます。シナプス小胞は情報の伝達を確保するために常にリサイクルされます。 シナプス小胞のリサイクルプロセスの最初の重要な段階には、ダイナミンというタンパク質による細胞膜の取り込みが関わっており、これによりシナプス小胞が切り取られます。このダイナミンは、一部、神経細胞の細胞骨格を構成する微小管に結合しており、他の細胞内プロセスにも関わっています。
ここで重要な拮抗物質はタンパク質「タウ」であり、正常な状態では微小管の安定に関わっています。しかし、アルツハイマー病の初期の段階では、タウは微小管から解離して、新たな微小管を過剰に生成させ、この微小管はダイナミンをサイトゾルから取り込んで、シナプス小胞の再生をブロックします。アルツハイマー病が進行すると、タウは凝集して神経原線維のもつれを形成します。神経原線維のもつれが生じると、アルツハイマー病と確定診断されます。
OISTの研究チームは、以前から特にダイナミンと微小管の相互作用に着目し、マウスの脳幹スライスを用いて合成ペプチドPHDP5がこの相互作用を阻害することを実証しました。現在OISTシナプス生物学ユニットに所属するザカリ・タウフィック博士(本論文の第二著者)は「以前eLifeに本チームの堀哲也博士らが報告したように、PHDP5は、ダイナミンと微小管の相互作用を阻害することで、PHDP5はダイナミンによる小胞のエンドサイトーシスと、これに続く小胞リサイクルを回復してシナプスを介する神経細胞間の失われたコミュニケーションを回復させることができるのです」と説明します。
研究チームは今回、トランスジェニックマウスを用いて、生体内でも同様の機能回復効果があることを証明しました。「PHDP5がマウスの学習・記憶障害を有意に改善したのを見て、私たちは興奮しました」とチャン博士は話します。「この成功により、アルツハイマー病の治療戦略として、ダイナミンと微小管の相互作用を標的とする可能性が見えてきました。」
研究チームは、この小型ペプチドPHDP5が血液脳関門を通過して海馬に到達できるようにするため、細胞膜透過性ペプチドを作製しました。このペプチドを血流に注入する代わりに 海馬に近く血液脳関門がよく発達していない鼻腔から投与することによって、海馬にペプチドが高濃度で到達し、全身投与による副作用の可能性を最小限にすると考えました。
分子と迷路から、実行可能な治療法へ
シナプスを比較的早い段階でPHDP5で治療すれば、ダイナミンと微小管の相互作用の暴走によるダメージを逆回転させ、治療を行ったトランスジェニックマウスが健常マウスと同等の学習・記憶能力を持つまでに回復させることができます。このペプチドでアルツハイマー病を治すことはできませんが、ダイナミンと微小管の相互作用が阻害されることで、認知機能の低下が大幅に遅延し、正常な寿命内であれば健康な人に影響を及ぼさない可能性があります。
この結果に勇気づけられた研究チームのスタッフは現在、別々のユニットに所属して研究を進めています。シナプス生物学ユニットに所属するタウフィック博士はペプチドの改良と投与方法の完成を目指しています。「副作用を最小限に抑えながら、脳内のPHDP5の量を増やし、より良い効果を得たいのです」とタウフィック博士は話します。彼が主導する研究チームはOISTの各分野のスペシャリストで構成され、治療法を改善するために様々な角度から取り組んでいます。神経計算ユニットに所属するチャン博士は、AIを実験に導入して、より強力なデータを獲得することを目指しています。「私たちは、OIST内の多様な専門分野を活用して研究を改善したいと思います」とチャン博士は話します。
実用化の面では、研究チームのスタッフはOIST Innovationと協力し、ペプチドを生産パイプラインに乗せるべく努力しています。「今後は製薬会社を巻き込みたいと考えています」タウフィック博士は話します。「製薬会社には薬理学の専門知識があり、私たちのペプチドを実用的な治療薬にするために必要なヒト試験を行うことができます。」
研究から医薬品になるまでの道のりは長く、論文執筆から薬が処方されるまで、平均20年かかります。しかし、研究チームは非常に意欲的です。チャン博士は「新型コロナワクチンは、科学的厳密性や安全性を犠牲にすることなく、治療法を迅速に開発できることを私たちに教えてくれました。そこまで早い実用化は期待しなくとも、各国、特に日本は、多くの人が罹患しているアルツハイマー病に対処したいと考えています。そして今、私達は、この研究を通じて、早期段階で治療すれば、認知機能の低下を効果的に回復させることが可能であることが分かりました」と話しています。
高橋智幸OIST名誉教授のコメント
高橋教授は、OISTを退職されましたが、このプロジェクトを立ち上げ、退職に伴いユニットが閉鎖されるまで主導されていました。「本研究では、アルツハイマー病におけるダイナミンと微小管(MT)の相互作用の病理学的意義を明らかにしました。ダイナミン-MT阻害剤PHDP5は、脳切片においてタウ蓄積によるシナプス機能障害を改善し、トランスジェニックアルツハイマー病マウスモデルにおいて学習・記憶障害を正常レベルまで回復させます。 この生体内効果は、二重盲検試験で再現性があり、2種類のモデルマウスで一貫していることから、強固なものです。明らかに、次の重要なステップは、PHDP5をアルツハイマー病治療臨床試験のフェーズ1-4試験に提出することです。私たちは、私たちが作製したペプチドがこれらの試験を通過し、それほど遅れることなくアルツハイマー病患者の手元に届き、患者やその家族の最大の関心事である認知症状を救うことを強く望んでいます。」
注
本研究は、2024年3月に閉鎖された細胞分子シナプス機能ユニットで開始されました。高橋智幸教授がプロジェクト全体の設計と指揮、論文の執筆を行い、グループリーダーの堀哲也博士は現在、タウフィック博士とともにシナプス生物学ユニットに所属し、実験セットアップや動物の手配、共同研究の組織化を行いました。チャジュ・チャン博士は行動実験を行い、ザカリー・タウフィック博士はペプチドの設計と改良を行いました。
論文情報
報道関係のお問い合わせ