クライオ電子顕微鏡をより使いやすく

ウイルス、タンパク質、その他の微小な生体分子の構造を視覚化することにより、生体分子がどのように機能するか、より深く理解することができます。このことが病気の新しい治療につながるかもしれません。 近年、クライオ電子顕微鏡技術と呼ばれる強力な技術により、急速凍結した試料をガラスのような氷に埋め込み、電子ビームで探ることで、生体分子イメージングの世界に革命をもたらしました。
しかしこの手法を使った顕微鏡は非常に高価であり、使用方法が複雑であるため、多くの研究者がアクセスできるものではありません。
沖縄科学技術大学院大学(OIST)の研究者らは、この問題に挑み、安価でより使いやすいクライオ電子顕微鏡を開発し、多くの研究者に手が届くようにしたのです。
この度OISTチームは、6年間のプロセスを経て、新しいイメージング機能を走査型電子顕微鏡に追加した顕微鏡を構築しました。 チームはこのハイブリッド顕微鏡を使用し、3つの異なる生体分子、2つの明確な形状のウイルスと1つのミミズのタンパク質のイメージングに成功しました。
「長く困難な道のりを経て今回のハイブリッド顕微鏡を構築できたことに大変満足しています。この顕微鏡は、より安価で使いやすいだけでなく、低エネルギー電子を利用しているため、画像のコントラストも改善される可能性があります。」と、量子波光学顕微鏡ユニット(新竹積教授)の研究者であり、Ultramicroscopy誌に発表された本研究の共同執筆者である安谷屋秀仁博士は述べています。

現在クライオ電子顕微鏡は、生体試料に高エネルギーの電子を発射することで機能します。 電子は生体分子内の原子と相互作用して散乱し、進行方向を変えます。 その後散乱電子は、検出器に当たり、特定の散乱パターンを用いてサンプルの画像を作成します。
しかし高エネルギーでは、電子が非常に早いスピードで突き抜けてしまうため、サンプル内の原子との相互作用が非常に弱く、この散乱は比較的少数しか発生しません。
「生体分子は、炭素、窒素、水素、酸素などの原子質量の低い元素で主に構成されています。これらの軽い元素は、高速電子には実質的には見えないのです。」と、論文共著者のマーティン・チャン博士は説明します。
これとは対照的に、低エネルギーの電子はゆっくりと移動するので、軽い元素とより強く相互作用を起こし、その結果、散乱事象がより頻繁に生じるのです。
しかし、この低エネルギー電子と軽い元素との間における強い相互作用については、標本を取り囲む氷の層においても電子を散乱させ、生体分子を取り巻くバックグラウンドノイズを生成してしまうため、利用することが困難です。
この問題を克服するため、研究者らは顕微鏡を調節し、異なるイメージング技術であるクライオ電子ホログラフィに切り替えました。

ホログラムの形成
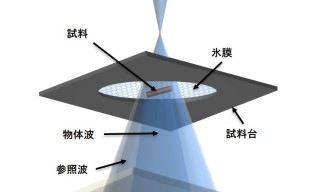
ホログラフィックモードでは、電子銃が低エネルギー電子のビームを試料に向けて発射し、電子ビームの一部が氷と試料を通過して物体波を形成する一方で、電子ビームの他の部分は氷のみを通過して参照波を形成します。 電子ビームの2つの部分は、池で波紋が衝突するように相互に作用し、明確な干渉パターン、つまりホログラムを形成します。

検出器はホログラムの干渉パターンに基づき、試料による散乱と氷膜による散乱を区別できるため、ビームの2つの部分を比較し、従来のクライオ電子顕微鏡では検出することが困難な電子からの追加情報を取得することも可能です。
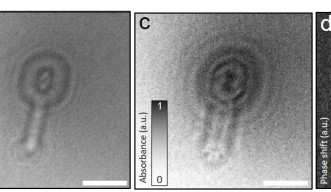
「電子ホログラフィは、振幅と位相という2種類の情報を提供してくれますが、従来のクライオ電子顕微鏡技術では位相しか検出できません」と、安谷屋博士は述べています。 すなわち、この追加情報により、試料の構造について、より多くの知識を得ることができるといいます。

薄い氷中でのブレークスルー
チームには、ハイブリッド顕微鏡を構築することのみならず、サンプル調製を最適化する必要もありました。 低エネルギー電子は、高エネルギー電子よりも氷によって散乱される傾向があるため、シグナルを最大化するには、試料を包む氷膜をできるだけ薄くする必要がありました。チームは水和酸化グラフェンの薄片を使用し、生体分子を所定の位置に保持し、より薄い氷の膜を形成できるようにしました。
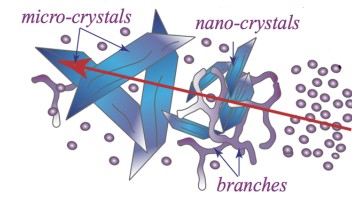
また、結晶氷の形成を防ぐために特別な措置を講じる必要がありました。「結晶氷の発生が、クライオ電子顕微鏡のイメージング技術にとっての弱点です。」とチャン博士はコメントします。

最新のセットアップと最適化された試料により、今回、ハイブリッドクライオ電子顕微鏡は最大数ナノメートルの解像度の画像を生成しました。ただ、この数値は、従来のクライオ電子顕微鏡で達成される、原子に近い解像度よりは、はるかに低いものではあります。
しかしながら、今回の顕微鏡技術は、分解能が今のまま高くはなくてもプレスクリーニング顕微鏡技術として需要があります。「低エネルギー電子は氷と非常に強く相互作用するために安価で使いやすい顕微鏡であり、研究者が従来のクライオ電子顕微鏡を使用して貴重な時間とお金を費やす前に、氷の品質を測定するのに役立ちます」と、安谷屋博士は説明します。
全体のプロセスも迅速で簡単です。 走査型(SEM)や走査透過モード(STEM)は、イメージングに最適なスポットを見つけた後、シームレスにホログラフィックモードに移行するのに役立ちます。 さらに、このモード切り替え技術を、市販の走査型電子顕微鏡に実装することができるため、今後この技術が広く採用されることが期待されます。
今後、チームは、電子銃をより高品質の電子ビームを生成するものに変更することにより、画像の分解能をさらに向上させることを目指して研究を進めていくと抱負を語っています。
専門分野
研究ユニット
広報・取材に関するお問い合わせ
報道関係者専用問い合わせフォーム