2018年10月19日
細胞の「微調整メカニズム」がエレガントな眼を作る
多細胞生物のさまざまな細胞がどのようにしてその個性を獲得するのかという問題は、今日の発生生物学においても、基本的で神秘的なテーマになっています。たとえば、眼の場合、水晶体は2種類の細胞、すなわち水晶体上皮細胞と水晶体線維細胞から構成されています。動物の成長とともに、水晶体上皮細胞は水晶体線維細胞に分化します。この分化の過程で、線維芽細胞増殖因子(FGF)が主要なアクセルとして働くことが以前から知られていました。この度、沖縄科学技術大学大学院(OIST)の研究チームは、FGFとは異なる分子シグナルがブレーキとして働き、分化すべきでないときに細胞が分化することを防ぐことを発見しました。
研究チームは、ヒトを含む脊椎動物と基本的に相同な構造の眼をもつゼブラフィッシュを用いて実験を行いました。2018年10月15日にDevelopment に発表された本研究は、細胞分化の複雑な過程に新たな洞察を示すものです。
「私たちは、水晶体のようなエレガントな構造が遺伝的なプログラムでどのように構築されるのか、解明したいと思っています」とOIST神経発生ユニットを主宰する政井一郎准教授は述べています。
本研究は、水晶体発生の仕組みを解明するだけでなく、ヒトの白内障手術で最も多く見られる合併症である後発白内障の原因を明らかにするために役立つことが期待されます。
既知の調整メカニズムの補完
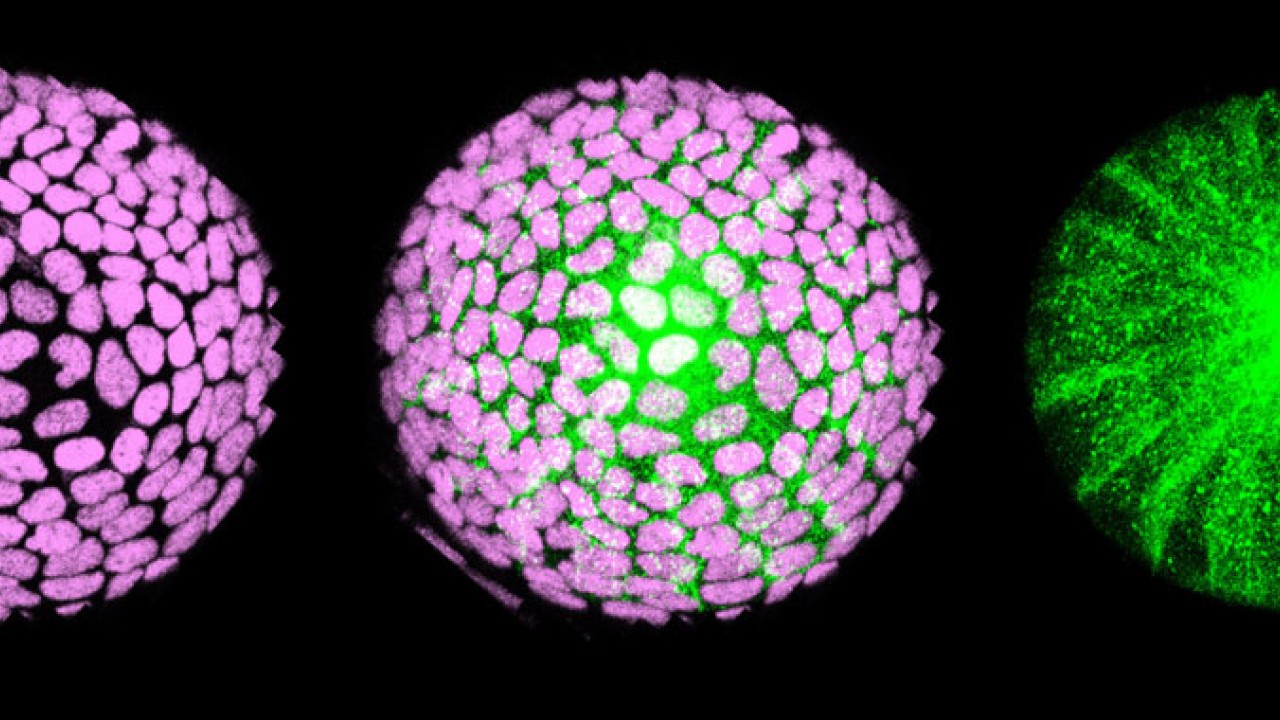
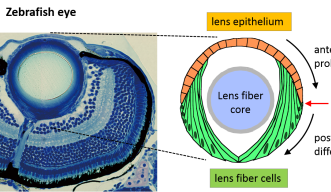
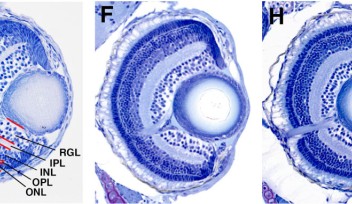
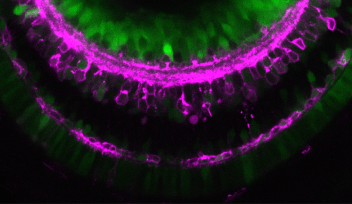
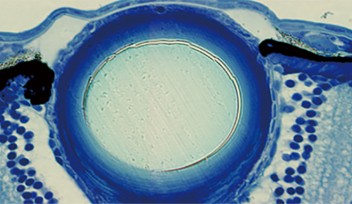
水晶体は球形で、その大部分は水晶体線維細胞で構成されています。これらの細胞は密集して配列し、お互いに隙間なく重なり合うことで硬い線維の核を形成しています。一方、水晶体上皮細胞は、一層の上皮として線維核の前側半球の表面を覆っています。発生過程において、水晶体上皮細胞は、増殖を繰りかえしながら、後方へ移動し、水晶体線維細胞に分化して、水晶体線維の核を外側から覆うことで一体化していきます。
水晶体上皮細胞から水晶体線維細胞への分化は、この移動の際、水晶体上皮細胞が「赤道」と呼ばれる明確な境界を通過する時点で開始します。水晶体上皮細胞がこのラインを超えると、分子レベルでの司令が働き、水晶体線維細胞への分化が進行します。このとき、重要な司令塔となる因子がFGFです。FGFは水晶体線維細胞への分化を促進しますが、政井准教授はこれを抑制する補完システムがあるのではないかと考えました。
「上皮細胞から線維細胞への切り替えは赤道上で生じ、その位置は非常に正確です。そのため、赤道で特異的に起こる線維細胞分化の開始を確実にするための微調整メカニズムがあるはずだと考えました。」と、政井准教授は言います。「おそらく、上皮細胞が赤道を通過すると、その分化抑制メカニズムから解放されることによって、線維細胞分化に入ることができるようになると考えました。」
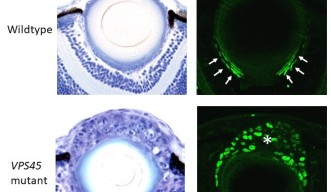
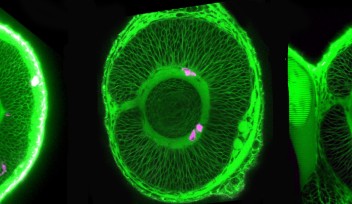
OIST神経発生ユニットでは、このような研究に適したゼブラフィッシュの突然変異体系統を維持しています。多数の変異体の中から、水晶体発生にユニークな異常を示す突然変異体を発見しました。通常、水晶体上皮細胞は単層の上皮を形成しますが、この変異体では、水晶体上皮細胞がランダムに積み重なった細胞塊になっています。この表現型は、赤道でのFGFシグナルの作用とは独立に、変異遺伝子によって、水晶体上皮細胞が赤道を通過する前に、線維細胞分化を引き起こすためであることが明らかになりました。
この変異遺伝子は通常、「液胞タンパク質選別関連タンパク質45」(VPS45)と呼ばれるタンパク質をコードしています。VPS45は、細胞膜から取り込まれた物質、おもにタンパク質を、分解に特化した細胞内小器官であるリソソームへ輸送したり、再利用のために再び細胞膜に戻したりする、例えば定期往復便をコーディネートするような役割を担っています。最近の研究から、この輸送システムは、細胞内のシグナル伝達経路を調節し、それにより発生過程を制御することが示唆されています。
実際、VPS45遺伝子に変異が生じると、水晶体上皮細胞を維持するシグナル経路が抑制され、線維細胞への分化を促進するシグナル経路が亢進することで、正常な水晶体発生が損なわれることが明らかになりました。
基礎生物学および白内障手術への応用
政井准教授の研究は、FGFと独立に水晶体線維細胞への分化を抑制するメカニズムが存在することを初めて示したことになります。現在、研究グループでは、水晶体発生においてVPS45が細胞のシグナル伝達をどのように制御しているのか、また、これらのシグナル経路は健全な発生をサポートするために、どのように協調して働くかについて、深く理解することを目指しています。この研究は、将来、VPS45のシグナル調節 がうまくいかないケースに必要な医学的な治療にも貢献する可能性があります。
例えば、今回の研究では、ゼブラフィッシュVPS45変異体ではTGF-βというシグナル伝達経路が活性化され、水晶体発生異常を引き起こすことが明らかになりました。また、TGF-βシグナル伝達は後発白内障の一因であることが報告されていますが、その詳細のメカニズムはまだ不明です。
白内障手術では、患者の濁った水晶体を取り除き、人工水晶体に置き換えます。手術で患者の視力は一旦回復しますが、水晶体上皮細胞が手術による損傷を受けて、自然治癒反応が起こることがあります。このとき、上皮細胞が傷を修復しようとして筋線維芽細胞または水晶体線維細胞に分化し、その結果、これらの細胞が人工水晶体を覆うことで透明性を損なう現象が、後発白内障です。水晶体発生を促進する因子をさらに深く理解することで、後発白内障を発症前に防止することができるかもしれません。
「このVPS45の基盤となるメカニズムを理解すれば、後発白内障の病理学的過程を抑制する治療法を開発につながる可能性があります」と、政井准教授は述べています。