2025年4月9日
人工進化が生んだ超高親和性 RNA–タンパク質ペアの構造基盤解明
【共同プレスリリース: 宮崎大学、九州大学、東京科学大学、OIST】
宮崎大学 テニュアトラック推進室 福永 圭佑 准教授(前東京科学大学特任助教)、九州大学 大学院農学研究院 寺本 岳大 助教、同角田 佳充 教授、 沖縄科学技術大学院大学(以下OIST) 核酸化学・工学ユニット 横林 洋平 教授、東京科学大学 地球生命研究所 松浦 友亮 教授らは、X 線結晶構造解析の手法を用いて二つの人工RNA−タンパク質複合体(RNP)の結合様式の違いを解明することに成功しました。さらに、これら RNP を活用した高性能リボスイッチ(遺伝子発現制御用の RNA スイッチ)の開発を行い、無細胞タンパク質合成系(セルフリーシステム)(注1)においてその性能の高さを実証しました。この研究成果は、2025 年3 月23 日に Oxford University Press のオープンアクセスジャーナル Nucleic Acids Research に掲載されました。
研究成果のポイント
- X 線共結晶構造解析により二つの人工RNP の結合様式の違いを原子レベルで解明
- タンパク質リガンドの結合によって翻訳が ON になるセルフリーシステム用リボスイッチを開発
- γ−ヘモリシンの機能発現を制御する論理回路(AND 回路)を構築
概要
CS1−LS4 および CS2−LS12 は PD-SELEX 法(注2)を使った実験室での共進化実験により同定された超高親和性・直交性(注3)の RNA−タンパク質(RBP)ペアです。 CS1−LS4、および CS2−LS12 複合体の X 線結晶構造解析を行ったところ、 これら RNA−RBP ペアはユニークな分子認識機構を獲得していたことが明らかとなりました。 また、 CS1-LS4 およびCS2-LS12 を分子パーツとして利用し、無細胞タンパク質合成系において翻訳制御が可能なセルフリーリボスイッチを 2 種類開発しました。このリボスイッチは LS4/LS12 が結合することにより翻訳が ON になる仕組みで、従来のセルフリーリボスイッチと比較して ON/OFF 比が大幅に向上していることが特徴です。さらに、リボスイッチを 2つ組み合わせることで二成分系の膜タンパク質γヘモリシンの機能発現制御を行うことにも成功しました。
背景
OIST の研究グループは RNA−RBP 間の結合様式を改変する手法として PD-SELEX(Phage Display coupled with Systematic Evolution of Ligands by EXponential enrichment)法を開発していました。合成生物学研究で一般的に分子パーツとして利用されている古細菌由来の L7Ae タンパク質とそれに結合するキンクターンRNA の結合選択性を改変することを目的に進化実験を行い、最終的に直交性を示す二組の RNA−RBP ペアCS1−LS4、及び CS2−LS12(解離定数はそれぞれ約7 pM)を取得することに成功しました。一方で、配列相同性の高いこれら RNA−RBP ペアがなぜ特異的にペアを作ることができるのかそのメカニズムは謎でした。このため今回、X 線共結晶構造解析により相互作用機構の解明に挑みました。
このような直交性 RBP−RBP ペアは生命科学研究のためのツール開発用の分子パーツとして有用ですが、これまでに CS1−LS4、 CS2−LS12 を利用した研究はあまり 報告されていません。 そこで今回、これら RNA− RBP ペアを利用して無細胞タンパク質合成系用の遺伝子発現制御ツール(リボスイッチ)の開発を行いました。
成果
今回、共同研究グループは X 線共結晶構造解析を行い人工 RNA−タンパク質複合体(RNP) である CS1−LS4 及 び CS2−LS12 の構造を決定することに成功しました(図1 )。 これら二つの RNP は祖先にあたるキンクターン RNA−L7Ae 複合体と 非常に似通った全体構造をしていることが分かりました。 一方で、 LS4/LS12 タンパク質に変異導入されたアミノ酸残基がπスタックや水素結合など異なる結合モードを介して CS1/CS2 RNA アプタマーを特異的に認識することが明らかとなりました。また、CS1/CS2 RNA はいずれもキンクターン様の構造を取 ることが分かりましたが、とりわけ CS1 RNA は非バルジ側のループが拡大、またグアニン塩基同士で非ワトソ ン−クリック塩基対を形成するなど、これまでに構造が解かれている天然のキンクターン RNA には存在しない特徴的な部分構造を持つこと を発見しました。さらに、LS12 は CS2 RNA 非存在下でホモ二量体を形成することを見出しました。二量体化は LS4 や祖先タンパク質 L7Ae には見られない性質であり、二量体化することで本来のパートナーではない低親和性のキンクターンRNAのアクセスを防ぐという新たなメカニズムが提唱されました。
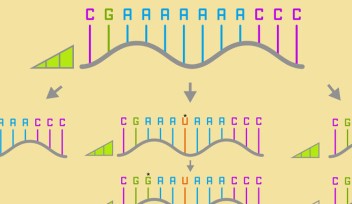
共同研究グループはさらに、無細胞転写・翻訳システムで機能するタンパク質リガンド応答型のリボスイッチ の開発に取り組みました(図2 )。 T7 プロモーター配列の直後に RNA アプタマー配列(CS1、または CS2) を挿 入し、転写時にタンパク質リガンド(LS4、 または LS12)が存在しない条件ではリボソーム認識配列を遮蔽することで、下流の遺伝子の翻訳が抑制されるようスイッチのデザインを行いました。タンパク質リガンドが存在する条件では、転写直後にタンパク質リガンドが結合のパートナーである RNA アプタマーと複合体を形成することでリボソーム認識配列がオープンになり 、リボソームによる翻訳(タンパク質合成)が行われます。つまり、タンパク質リガンドが存在する条件でのみタンパク質合成が行われる ON スイッチを作製しました。蛍光タンパ ク質(EGFP)レポーターの発現レベルを指標にしたスクリーニングにより、ON/OFF 比 500 に匹敵する世界最高性能のセルフリーリボスイッチを同定することに成功しました。これまでに、低分子やタンパク質などのリガンドに応答するセルフリーリボスイッチが報告されてきましたが、ON/OFF 比が 3 桁を超えるものは知られていません。本研究では、3 桁の ON/OFF 比を示す直交性リボスイッチ二組を開発することに成功しています。
γヘモリシンは Hlg2 および LukF から構成される二成分系の膜タンパク質であり、赤血球にナノポアを形成することで溶血を引き起こします。一成分系のαヘモリシンは無細胞(セルフリー)合成生物学、とりわけ人工細胞を用いた研究において利用されることが多い膜タンパク質ですが、γヘモリシンを使った研究例はありませんでした。今回開発した二つのリボスイッチを用い、 セルフリー系において LS4・ LS12 二つのタンパク質リガンドが存在する条件でのみγヘモリシンが機能発現する論理回路(AND 回路)の構築を行いました。ヘモリシンの活性を高感度に検出することが可能なウサギ赤血球を用いて溶血アッセイを行ったところ、LS4・ LS12 が存在する条件でのみ溶血が観察され、AND 回路が機能していることが示されました(図3 )。同様に、人工脂質二重膜(LUVs)を用いた実験系においても、AND 回路を使ったγ−ヘモリシンの機能発現制御を行うことに成功しています。γヘモリシンがセルフリー系において機能を持つ形で合成できることを示したのは新たな知見です。
展望
CS1−LS4、CS2−LS12 の構造解析によりこれら RNP における相互作用の違い、また共通する相互作用が明らかとなりました。今後、RNP 間の直交性をさらに向上させるため、分子・ライブラリーのデザインに構造情報が活用されることが期待されます。また今回、CS1−LS4、CS2−LS12 を用いることで 3 桁の ON/OFF 比を示す高性能セルフリーリボスイッチを開発することに成功しましたが、さらなる ON/OFF 比の向上を目指し、カスケード回路の構築などを進めています。 これら RNA−RBP ペアが大腸菌・ 動物細胞など異なるプラットフォーム(生細胞)で機能するのかも今後の検証課題の一つです。
発表者
宮崎大学 テニュアトラック推進室: 福永 圭佑(准教授) 九州大学 大学院農学研究院:寺本 岳大(助教) 、 中島 もも香(大学院生)、 角田 佳充(教授) 東京科学大学 地球生命研究所: 福永 圭佑(特任助教, 研究当時)、 大谷 俊貴(大学院生)、松浦 友亮(教授) 沖縄科学技術大学院大学 核酸化学・工学ユニット:福永 圭佑(ポストドクトラルスカラー, 研究当時)、横林 洋平(教授) 電気通信大学 大学院情報理工学研究科:勝木 陸(大学院生)
用語解説
(注1) 無細胞タンパク質合成系(セルフリーシステム) 転写に必要な RNAポリメラーゼや翻訳に必要なリボソームなどタンパク質合成に必要な成分を含む反応液であり、 DNA/mRNA を追加するだけでタンパク質が合成される。 近年、セルフリーシステムを用いた無細胞合成生物学研究が盛んに行われている。
(注2)PD-SELEX 法 ファージディスプレイライブラリー ×RNA ライブラリーのセレクションを行う共進化分子工学の手法。 タンパク質を提示するファージライブラリーと RNA ライブラリーを構築し、試験管内で結合する RNA−RBP ペアのみを選択・増幅するという操作を繰り返すことが特徴。 論文に詳細が掲載されています。
論文情報
研究ユニット
報道関係のお問い合わせ