2018年6月1日
「きっとうまくいく」未来を信じる力を支えるセロトニン
概要
沖縄科学技術大学院大学(OIST)の研究員らは、マウスの脳内で神経伝達物質であるセロトニンを放出する神経細胞の活動(セロトニン神経活動※1)を活性化すると、「報酬のエサを獲得できる可能性が高いが、それをいつ獲得できるかわからない」という状況下で報酬をより長く待てるようになることを見出しました。さらに数理モデルを用いたシミュレーションで、セロトニンの活性化が報酬を獲得できる確信度を高めるとすると、結果の確実さとタイミングの不確実さに対する影響を統一的に説明できることを明らかにしました。
いつ結果が得られるかわからないという時間的不確実性のもとで報酬をめざす行動をセロトニンが促進するという本研究による知見は、うつ病などの精神障害において、認知行動療法とあわせることで、いつ回復するか予測不能な治療を継続するための辛抱強さを効果的に高め、患者が回復途中に治療から脱落するのを防ぐことに貢献する可能性があります。
論文は、英科学誌 Nature Communications(ネイチャー・コミュニケーションズ)に掲載されました。
研究の背景と経緯
人気のお店で並んだり、海で釣り糸を垂らして大物を狙って待ち続けたりするなど、私たちの生活で「辛抱強さ」が必要とされる場面は多く存在します。将来的に予測される報酬のために、焦らず辛抱強く待つことが求められる時、どのような脳内メカニズムがそれを可能にするのでしょうか?
OIST神経計算ユニットの宮崎勝彦研究員、宮崎佳代子研究員、銅谷賢治教授は、光によって脳内の特定の神経細胞の活動を正確なタイミングで制御する「光遺伝学※2」の手法を取り入れたマウス実験により、セロトニン神経の起始核※3の一つである背側縫線核※4のセロトニン神経細胞を刺激することで、将来報酬が与えられる小窓に鼻先を入れるノーズポークという行動(報酬待機行動)が、より長く持続されることを報告してきました。※5
将来的に予測される報酬のために辛抱強く待てることは、その報酬を獲得できる機会を増大させます。一方で、あまり確実ではない報酬を持ち続けることは、時間や体力を浪費し得策ではありません。このように将来の報酬に対する確かさ(確信度)に基づいて行動を柔軟に切り替えることが、より多くの報酬を獲得するうえで大切です。
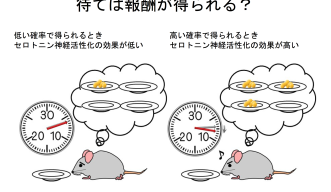
そこで今回、研究グループは、セロトニンが将来得られる報酬の確実さの予測に応じて辛抱強さの調節に関与していると考え、報酬の確率を変化させた場合と、獲得できるタイミングの確実さを変化させた場合に、報酬待機行動に対するセロトニン活性化の効果がどのように変化するかを詳細に調べ、以下の結果を見出しました。
- セロトニン神経の活性化は、75%の確率で獲得できる報酬の待機時間を延長するが、50%または25%の確率で獲得できる報酬の待機時間を延長しない。
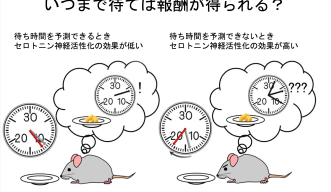
- 75%の確率で獲得できる報酬が、獲得できる時間が不確実になると、確実に予測可能な場合に比べて待機行動に対するセロトニン活性化の効果が増加する。
- 数理モデルを用いたシミュレーションの結果、セロトニンの活性化が将来獲得できる報酬の確信度を高めるとすると、報酬獲得の確実さとタイミングの不確実さの影響を再現することができる。
研究内容
1. セロトニンの待機促進効果は報酬の確率に依存する
実験では、7匹のマウスに、実験箱内部の壁面に設置された小窓にノーズポーク(鼻先を入れる)した状態で数秒間じっと待つことでエサを獲得できる課題を学習させました。マウスにはノーズポークをする習性がありますが、通常はすぐに鼻先を出してしまいます。今回の課題ではノーズポークを一定時間続けるとエサを獲得できるため、マウスはノーズポークを続けました。待ち時間を3秒とし、75%の確率で報酬を獲得できる課題、25%の確率で報酬を獲得できる課題でそれぞれの半数の試行で背側縫線核のセロトニン神経細胞を光で刺激しました。この時、事前の合図はなく、待ち時間やエサの有無は待ってみないとわかりません。チームは、報酬が出ない試行に注目してマウスのノーズポーク時間を計測しました。その結果、75%報酬の課題では、セロトニンを活性化するとノーズポーク時間が約7秒から約8秒に延長しました。それに対し、25%報酬の課題では、セロトニンを活性化してもしなくてもノーズポーク時間は約6秒と変化しませんでした(図1)。50%報酬の課題でもノーズポーク時間に対するセロトニンの効果は見られませんでした。
2. 報酬の時間的不確実性はセロトニンの待機促進効果を増大させる
次に、報酬が獲得できることはかなり確実だが(75%の確率)、いつ獲得できるかが予測できない時に(時間的不確実性が大きい)、報酬待機に対するセロトニンの効果を調べました。ここでは、エサが必ず6秒後に出る課題、エサが2、6、10秒後のいずれかで出る課題でそれぞれの半数の試行でセロトニン神経細胞を光で刺激し、報酬が出ない試行時のノーズポーク時間を計測しました。その結果、エサが必ず6秒後に出る課題では、セロトニンの活性化はノーズポーク時間を約11秒から約12秒へ約10%延長しました。それに対し、エサが2、6、10秒後のいずれかで出る課題では、セロトニンの活性化はノーズポーク時間を約13秒から約18秒へ30%以上延長しました(図2)。
3. セロトニンの活性化は将来報酬の確信度を高めることで辛抱強さを促進する
それではセロトニン神経の活性化はどのように報酬待機行動の促進を調節しているのでしょうか?研究グループは、マウスはエサが出るとするといつ頃出るという確率分布を学習しており、長く待ってもエサが出ないと今回はエサあり試行である確率(尤度)が低下するという数理モデルを用いて実験結果を再現する条件をシミュレーションしました。その結果、セロトニン神経の活性化は、エサあり試行の確率が大きいときにそれをさらに大きく予測する(報酬試行の事前確率を増大させる)と仮定すると実験結果を再現できることが分かりました。例えば(2)の実験では、エサの出るタイミングが不確実なほどエサあり試行の事前確率の効果が大きくなり、セロトニン神経活性化により報酬の確信度が増大すると、エサなし試行であるという判断がより遅くなります。この結果は、セロトニン神経の活性化によって、なかなかエサが出ないという現実よりも、きっとエサがでるはずだという確信に基づいて判断を行う、つまり、より楽観的になることで、マウスはより長く報酬を待つようになると考えられます。
今回の研究成果のインパクト・今後の展開
本研究成果は、セロトニン神経の活性化だけでは辛抱強く待つことを促進するのに十分ではなく、将来の報酬に対する主観的確信度が高いことが必要であることを示唆しています。このことは、精神疾患治療での応用につながる可能性があります。例えば、選択的セロトニン再取り込み阻害薬(SSRI)は、脳全体のセロトニンの作用を高めることによって精神障害、特にうつ病を治療するために広く使用されています。しかし、SSRI治療だけでは症状が落ち着く寛解率が約40%に留まっているのに対し、SSRI治療と組み合わせた認知行動療法などの心理的治療は、薬物治療単独よりも高い改善率を示しています。今回研究チームは、辛抱強さを促進するのにセロトニン神経のみの活性化だけでは不十分であり、目標に対する主観的確信(すなわち、高い将来の報酬確率)が必要であることを明らかにしました。この発見は、セロトニンの作用を高めるSSRI治療と患者の悲観的認知を変更する認知行動療法の併用効果を説明するかもしれません。また、認知行動療法の効果は緩やかで、患者にとっていつ回復できるかを予測することは困難だと思われます。報酬の時間的不確実性に対するセロトニンの待機促進効果の知見は、SSRI治療によるセロトニンの増強が、いつ回復するか予測不可能な治療を継続するための辛抱強さを効果的に高め、患者が回復途中に治療から脱落するのを防ぐことに貢献する可能性も考えられます。
論文筆頭著者の一人、宮崎勝彦博士は「今後、脳のどの領域にセロトニンが働くことで辛抱強さの促進に寄与しているのかを明らかにする予定です。背側縫線核は前脳に広く投射し神経終末でセロトニンを放出しています。ある特定の領域に投射するセロトニンが重要であることが解明されれば、特定の領域のセロトニンだけを増強する副作用の少ない薬の開発などに貢献できることが期待されます。」と、今後の展開を語っています。
用語説明・参考論文
※1 セロトニン神経活動
脳内で神経伝達物質であるセロトニンを放出する神経細胞の活動のこと。セロトニン神経活動により神経終末からセロトニンが放出され、ほかの神経細胞にセロトニン受容体を介して作用する。
※2 光遺伝学
神経回路機能を調べるため光学と遺伝学を融合した研究分野。光活性化イオンチャンネルであるチャネルロドプシン2などを特定の神経細胞に遺伝子工学的手法を用いて強制的に発現させた後、標的神経細胞に特定の波長の光を照射することで神経活動をミリ秒単位の時間制度で操作することができる。
※3 起始核
神経核のうち遠心性ニューロンの細胞体がある部分。反対に、終止核は、神経核のうち求心性ニューロンがシナプス結合をつくるニューロンがある部分。
※4 背側縫線核
脊椎動物の中脳に存在する脳部位。大脳の前部の広い範囲に投射し、脳の活動を調節しているセロトニン神経細胞を含んでいる。背側縫線核のセロトニン神経細胞は、睡眠―覚醒サイクル、運動調節、気分障害、衝動性などに関係していると考えられている。
※5参考論文:Miyazaki et al. "Optogenetic Activation of Dorsal Raphe Serotonin Neurons Enhances Patience for Future Rewards” DOI: https://doi.org/10.1016/j.cub.2014.07.041
プレスリリース(PDF)