2016年7月21日
本物の薬をバーチャルで開発
体内では、ひとつの薬が複数の分子と相互作用をすることが可能です。この現象は「多重薬理学」と呼ばれており、その薬の相互作用の仕方によって、病気を治癒したり、副作用を引き起こしたりします。このため、好ましくない分子相互作用のリスクを減らしながら、標的となる分子に作用する薬を開発することが重要です。通常、研究室での膨大な実験によりこのような選択的相互作用をもつ薬剤を見つけます。新薬候補の化合物は、効果や特異性を確認するため、長期にわたる様々な検査を経なければならず、このプロセスには多くの時間と費用がかかります。
この度、日本国内の複数の研究機関に所属する研究者たちが、こうした状況に革命をもたらすオンラインシステムを開発しました。沖縄科学大学院大学(OIST)、システムバイオロジー研究機構、東京大学、理化学研究所総合生命医科学研究センターが共同開発した、新薬候補の化合物の効果と特異性を仮想空間内で確認するためのsystemsDockです。このシステムはインターネット上で誰でも無料で利用することができます。本プロジェクトにおいて、OISTのITセクションは基盤となる技術サポートを行いました。その成果はNucleic Acids Researchに掲載されています。
論文筆頭著者であり、OISTの統合オープンシステムユニットのスタッフサイエンティストであるクンイー・シーン博士は以下のように説明します。「新たな薬を産み出すプロセスは、すべてがスムーズに進んだとしても軽く10年はかかります。有望な化合物を見つけたとしても、その化合物は複数の生体分子と相互作用してしまいます。結果として副作用を起こすことがあり、患者はその副作用で命を落としたり、副作用をおそれてそもそも薬を使うことができない場合もあるのです。典型的な副作用として心毒性が挙げられます。」
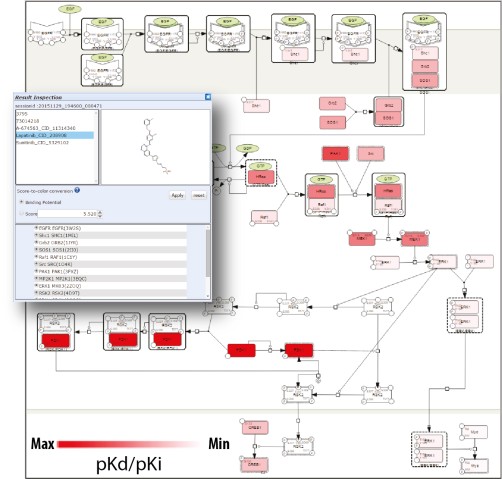
systemsDockは、将来薬となる可能性を持つ化合物と生体内のターゲット分子の間での相互作用を、効果的かつ実践的に、バーチャルにスクリーニングする目的で作られました。このオンラインシステムを使用すると、その新薬候補の化合物が体内の分子とどのように「ドッキング」するか、すなわち、どのように結合するかを予測することができます。systemsDockを開発するにあたり、研究者はこのドッキング予測の精度を大幅に改良しました。このドッキング予測技術こそ、薬剤と生物分子の間の相互作用を予測するために必要不可欠な技術なのです。
また、ドッキングの予測精度が改善されたことだけが、この研究ツールの特徴ではありません。シーン博士は付け加えます。「ドッキングの予測をするオンラインリソースは他にもあります。しかしそれらのウェブサイトでは、通常、ユーザーはひとつの生体ターゲットに対して様々な薬剤のスクリーニングを行います。systemsDockでは、多くの新薬候補化合物と多くの生体ターゲット間でのスクリーニングを、一括して行うことができるのです。」
さらにsystemsDockでは、 より広い意味での“生物学的システム”の中で薬剤と生体分子間の相互作用について調べることが可能です。その生物学的システムの中で生体分子間の相互作用が生じているのです。「システム生物学は比較的新しい分野です。複数の異なる生物学的システムをひとつに統合することで、全体を大きなひとつのシステムとして捉える、というのがシステムバイオロジーの基本的な考え方です。統合されたシステムは生体分子の地図のようになるのです。」と、シーン博士は説明を加えます。これらの地図を活用することでsystemsDockはより包括的なスクリーニングを行うことができ、薬剤と生物システムの相互作用をより深く理解することに役立つのです。
ある生物学的機能に関する地図を新たに作り出すことは、長ければ3年もかかる大変な試みです。「本来は長い年月と多大な努力を必要としますが、システムバイオロジー研究所の生物学的地図を作成する専門家と共同開発することで、このような素晴らしいツールを提供することになったのです。」と、シーン博士は熱く語ります。アルツハイマーやパーキンソン病、インフルエンザといった特定の疾病にフォーカスを当てた地図が既に作成されており、 それらをsystemsDockで使用することができます。
複数の薬剤と複数の生体ターゲットでは、多くの相互作用が生じるので、スクリーニングのプロセスの結果は複雑です。しかしsystemsDockは、相互作用の予測結果の可視化にも工夫が凝らされており、楽に行うことができます。異なる分子や薬剤の間での相互作用のタイプに応じて、結合を示す色を変えて、地図上でナビゲーションできるのです。また、化合物や生体ターゲットの3次元構造を表示する機能も併用することで、このようなシステムの操作に不慣れな科学者であってもsystemsDockを直感的に使うことができます。
シーン博士は強調します。「systemsDockは、 薬剤を開発するためにかかる時間やリソースを削減しつつ、新薬として有望な化合物を発見することができます。また、エラーが生じる確率を低減でき、薬剤開発プロセス全体にとっての利益となるのです。」